详情
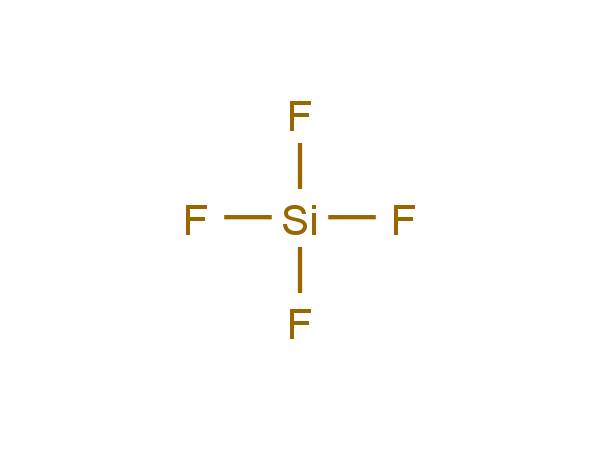
中文名称: 四氟化硅 英文名称: silicon tetrafluoride
中文名称2: 氟化硅
Si原子以sp3杂化轨道形成σ键。分子形状为正四面体形。
英文名称2: silicon fluoride
CAS No.: 7783-61-1
分子式: SiF4
分子量: 104.06
理化特性
主要成分: 纯品
外观与性状: 无色、有毒、有刺激性臭味的气体,易潮解,在潮湿空气中可产生浓烟雾。
熔点(℃): -90.2(175.6kPa)
沸点(℃): -65(24.1kPa)
相对密度(水=1): 4.67
相对蒸气密度(空气=1): 3.6
临界温度(℃): -14.06
临界压力(MPa): 3.72
溶解性: 溶于乙醇、醚、硝酸、氢氟酸。
主要用途: 用于氟硅酸及氟化铅的制取,也用作水泥和人造大理石的硬化剂,有机硅化合物的合成材料。
健康危害: 本品对眼、皮肤、粘膜和呼吸道有严重损害。局部腐蚀作用强。严重中毒者可致肺炎、肺水肿。
燃爆危险: 本品不燃,有毒,具腐蚀性、刺激性,可致人体灼伤。
危险特性: 在潮湿空气中产生白色有腐蚀性和刺激性的氟化氢烟雾。遇水缓慢水解硅酸及氟化氢。
四氟化硅在潮湿的空气中因水解而产生烟雾,生成硅酸和氢氟酸二氧化硅与氢氟酸反应则生成气态四氟化硅:SiO2(s) + 4 HF(aq) → SiF4(g) + 2 H2O(l)
与碳酸钠溶液发生不完全水解反应:3SiF4+2Na2CO3+2H2O=H4SiO4↓+2Na2SiF6↓+2CO2
与 氢氧化钠反应较为彻底;SiF4+6NaOH=Na2SiO3+4NaF+3H2O
与氢氟酸生成氟硅酸(六氟合硅酸)SiF4+2HF=H2SiF6
中文名称2: 氟化硅
Si原子以sp3杂化轨道形成σ键。分子形状为正四面体形。
英文名称2: silicon fluoride
CAS No.: 7783-61-1
分子式: SiF4
分子量: 104.06
理化特性
主要成分: 纯品
外观与性状: 无色、有毒、有刺激性臭味的气体,易潮解,在潮湿空气中可产生浓烟雾。
熔点(℃): -90.2(175.6kPa)
沸点(℃): -65(24.1kPa)
相对密度(水=1): 4.67
相对蒸气密度(空气=1): 3.6
临界温度(℃): -14.06
临界压力(MPa): 3.72
溶解性: 溶于乙醇、醚、硝酸、氢氟酸。
主要用途: 用于氟硅酸及氟化铅的制取,也用作水泥和人造大理石的硬化剂,有机硅化合物的合成材料。
健康危害: 本品对眼、皮肤、粘膜和呼吸道有严重损害。局部腐蚀作用强。严重中毒者可致肺炎、肺水肿。
燃爆危险: 本品不燃,有毒,具腐蚀性、刺激性,可致人体灼伤。
危险特性: 在潮湿空气中产生白色有腐蚀性和刺激性的氟化氢烟雾。遇水缓慢水解硅酸及氟化氢。
四氟化硅在潮湿的空气中因水解而产生烟雾,生成硅酸和氢氟酸二氧化硅与氢氟酸反应则生成气态四氟化硅:SiO2(s) + 4 HF(aq) → SiF4(g) + 2 H2O(l)
与碳酸钠溶液发生不完全水解反应:3SiF4+2Na2CO3+2H2O=H4SiO4↓+2Na2SiF6↓+2CO2
与 氢氧化钠反应较为彻底;SiF4+6NaOH=Na2SiO3+4NaF+3H2O
与氢氟酸生成氟硅酸(六氟合硅酸)SiF4+2HF=H2SiF6





 豫公网安备 41030202000092号
豫公网安备 41030202000092号 网站首页
网站首页 电话咨询
电话咨询 返回顶部
返回顶部